ĄĄĄĄČËĩÄÎļŌšÖКŽÓÐû}ËáĢŽÆûÜģĢÓÃĩÄëÆŋ(ÐîëģØ)ÖÐÓÐÁōËáČÜŌš��ĢŽĘģīŨÖКŽÓÐ3%ĄŦ5%ĩÄīŨËáĢŽËáÓęÖКŽÓÐOÉŲÁŋĩÄÁōËášÍÏõËá����ĄĢû}ËáĄĒÁōËá��ĄĒÏõËá����ĄĒīŨËášÍĖžËáĘĮŨîģĢŌĩÄŨ·NËá�ĄĢļųþ(jĻī)ģõÖÐŧŊW(xuĻĶ)ÖŠŨRĢŽÎŌÖŠĩĀËáŌŧ°ãūßÓÐŌÔÏÂÍĻÐÔĢš
ĄĄĄ����ĄĒŲÅcÅÅÔÚ―ðŲŧîÓíÐōąíHÖŪĮ°ĩÄ―ðŲ·īŠ(yĻĐng)Ūa(chĻĢn)Éúû}šÍäâ;
ĄĄĄ����ĄĒÚÅcA°l(fĻĄ)ÉúÖКͷīŠ(yĻĐng)ÉúģÉû}šÍËŪ;
ĄĄĄ�ĄĒÛÅcĖžËáâ}ĄĒĖžËáâc·īŠ(yĻĐng)Ūa(chĻĢn)ÉúķþŅõŧŊĖž�����ĄĒËŪšÍÐÂû};
ĄĄĄ���ĄĒÜÅc―ðŲŅõŧŊÎï·īŠ(yĻĐng)ÉúģÉû}šÍËŪ;
ĄĄĄ���ĄĒÝÄÜĘđËáAÖļĘūĐŨÉŦĄĢ
ĄĄĄĄ[ÔŌŧÔ]ĄĄ1.ŌÔÏĄÁōËáéĀý�ĢŽļũÅeŌŧĀýŧŊW(xuĻĶ)·īŠ(yĻĐng)·―ģĖĘ―ÕfÃũÆäŌŧ°ãÐÔŲ|(zhĻŽ)ĄĢ
ĄĄĄĄäŅõŧŊâcËŨ·QýA����ĄĒŧðAŧōŋÁÐÔâcĢŽäŅõŧŊâ}ËŨ·QÏûĘŊŧŌŧōĘėĘŊŧŌ��ĢŽNH3·H2OĘĮNH3ĩÄËŪČÜŌš��ĢŽžī°ąËŪĢŽËüķžĘĮģĢŌĩÄA��ĄĢļųþ(jĻī)ģõÖÐŧŊW(xuĻĶ)ÖŠŨR�ĢŽÎŌÖŠĩĀAŌŧ°ãūßÓÐŌÔÏÂÍĻÐÔĢš
ĄĄĄĄĒŲÅcËá°l(fĻĄ)ÉúÖКͷīŠ(yĻĐng)ÉúģÉû}šÍËŪ;
ĄĄĄ�����ĄĒÚÅcCO2·īŠ(yĻĐng)ÉúģÉû}šÍËŪ;
ĄĄĄ�ĄĒÛÅcCuCl2ĩČû}·īŠ(yĻĐng)ÉúģÉÐÂû}šÍÐÂA;
ĄĄĄĄĒÜÄÜĘđËáAÖļĘūĐŨÉŦ����ĄĢ
ĄĄĄĄ[ÔŌŧÔ]ĄĄ2.ŌÔäŅõŧŊâ}éĀýĢŽļũÅeŌŧĀýŧŊW(xuĻĶ)·īŠ(yĻĐng)·―ģĖĘ―ÕfÃũÆäŌŧ°ãÐÔŲ|(zhĻŽ)�����ĄĢ
ĄĄĄĄû}ĘĮÎŌÃŋĖėķžëxēŧé_ĩÄÕ{(diĻĪo)ÎķÆ·��ĢŽÉúŧîÖÐĩÄû}ĘĮÖļĘģû}��ĢŽŌēūÍĘĮÂČŧŊâc�����ĢŽŧŊW(xuĻĶ)W(xuĻĶ)ŋÆÖÐĩÄû}ĘĮÖļÓÉAĩÄęëxŨÓšÍËáĩÄęëxŨÓ―MģÉĩÄŧŊšÏÎï�ĄĢÎŌÔÚÉúŪa(chĻĢn)ĄĒÉúŧîÖÐ―(jĻĐng)ģĢÓÃĩ―ļũ·NļũÓĩÄû}��ĢŽČįĘģû}�����ĄĒĖžËáâ}(īóĀíĘŊ)�ĄĒÁōËáäXĄĒĖžËáäâc(ÐĄĖKīō)�ĄĒÁōËáä@ĄĒĖžËáää@ĩČĩČ�ĄĢŌŧ°ãíÕfĢŽû}ŋÉŌÔšÍËá�����ĄĒA���ĄĒÆäËûû}°l(fĻĄ)ÉúŧŊW(xuĻĶ)·īŠ(yĻĐng)����ĢŽēŧÍŽ―MģÉĩÄû}ÐÔŲ|(zhĻŽ)ļũēŧÏāÍŽ��ĄĢ
ĄĄĄĄķþŅõŧŊĖžĄĒŅõŧŊæV�����ĄĒËÄŅõŧŊČýčFĩČĘĮÓÉÉ·NÔŠËØ―MģÉĩÄŧŊšÏÎï����ĢŽÆäÖÐŌŧ·NÔŠËØĘĮŅõĢŽß@ÓĩÄŧŊšÏÎï―ÐŨöŅõŧŊÎï��ĄĢēŧÍŽĩÄŅõŧŊÎïÐÔŲ|(zhĻŽ)ļũēŧÏāÍŽ�����ĢŽČįCuOÄÜšÍËá·īŠ(yĻĐng)��ĢŽCO2žČÄÜšÍA·īŠ(yĻĐng)ÓÖÄÜšÍËŪ·īŠ(yĻĐng)���ĄĢ
ĄĄĄĄDøð^ĀïÓÐÔSÔSķāķāĩÄøžŪ���ĢŽéĘēÃīÄãÄÜōšÜŋėūÍÕŌĩ―ÄãËųÐčŌŠĩÄDø?īóÐÍģŽĘÐĀïÓÐģÉĮ§ÉÏČf·NÉĖÆ·ĢŽéĘēÃīÄãÄÜōŅļËŲĖôģöÄãËųÐčŌŠĩÄÉĖÆ·?ß@ĘĮŌō?yĻĪn)éČËÔÚĒß@ÐĐøžŪŧōÉĖÆ·ęÁÐĩ―øžÜŧōØžÜÖŪĮ°�ĢŽŌŅ―(jĻĐng)ĘÂÏČĶËüßM(jĻŽn)ÐÐÁË·ÖîĖĀíĄĢ°ŅīóÁŋĘÂÎï°īÕÕĘÂÏČÔO(shĻĻ)ķĻĩÄ“Ë(biĻĄo)Ę(zhĻģn)”ßM(jĻŽn)ÐзÖîĢŽĘĮČËŨîĘėÏĪ�����ĢŽŌēĘĮŨî·―ąãĩÄŌŧ·NđĪŨũ·―·Ļ�ĢŽß@·N·―·ĻÔÚÉįþÉúŧî��ĄĒ―(jĻĐng) IđÜĀíšÍŋÆW(xuĻĶ)žžÐg(shĻī)ÖÐĩÃĩ―ÁËV·šĩÄŠ(yĻĐng)ÓÃ���ĄĢ
ĄĄĄĄ―(jĻĐng)ß^ĘÕžŊĀýŨCšÍËžËũ�ĢŽÎŌŋÉŌÔ°l(fĻĄ)ŽF(xiĻĪn)·Öî·ĻŠ(yĻĐng)ÓÃĩÄÆÕąéÐÔ�ĄĢŪ(dĻĄng)·ÖîĩÄË(biĻĄo)Ę(zhĻģn)ī_ķĻÖŪšóĢŽÍŽîÖÐĩÄĘÂÎïÔÚÄģÐĐ·―ÃæĩÄÏāËÆÐÔŋÉŌÔÍÖúÎŌŨöĩ―ÅeŌŧ·īČý;ĶÓÚēŧÍŽîĘÂÎïĩÄÁË―âĘđÎŌŨöĩ―ÓÉīËž°ąË���ĄĢËųŌÔ·Öî·ĻĘĮŌŧ·NÐÐÖŪÓÐЧ�����ĢŽšÎŌŨÐÐĩÄŋÆW(xuĻĶ)·―·Ļ�ĄĢÉúÎïW(xuĻĶ)ÖаŅÓÖēÎï°īÕÕ―į����ĄĒéTĄĒūVĄĒÄŋ�ĄĒŋÆĄĒŲ�ĄĒ·NßM(jĻŽn)ÐзÖîĩÄ·―·ĻĘĮŨîÓÐīúąíÐÔĩÄ(shĻŠ)ĀýÖŪŌŧĢŽĶÉúÎïW(xuĻĶ)ĩÄ°l(fĻĄ)ÕđÆðĩ―ÖØŌŠŨũÓÃ��ĄĢ
ĄĄĄĄĶÓÚĩ(shĻī)ŌÔĮ§ČfÓ(jĻŽ)ĩÄŧŊW(xuĻĶ)ÎïŲ|(zhĻŽ)šÍéĩ(shĻī)ļüķāĩÄŧŊW(xuĻĶ)·īŠ(yĻĐng)����ĢŽ·Öî·ĻĩÄŨũÓÃŨšõĘĮoŋÉĖæīúĩÄĄĢĀýČį��ĢŽÔÚģõÖÐŧŊW(xuĻĶ)ÖÐ���ĢŽÎŌÔø―(jĻĐng)°ŅÔŠËØ·Öé―ðŲÔŠËؚͷĮ―ðŲÔŠËØ����ĢŽ°ŅŧŊšÏÎï·ÖéËá�ĄĒAĄĒû}šÍŅõŧŊÎï���ĢŽ°ŅŧŊW(xuĻĶ)·īŠ(yĻĐng)·ÖéŧŊšÏ·īŠ(yĻĐng)�ĄĒ·Ö―â·īŠ(yĻĐng)��ĄĒÖÃQ·īŠ(yĻĐng)šÍÍ(fĻī)·Ö―â·īŠ(yĻĐng)ĩČĩČĄĢ
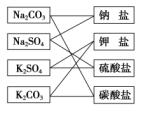
ĄĄĄĄÓÉÓÚŌŧ·N·Öî·―·ĻËųŌĀþ(jĻī)ĩÄË(biĻĄo)Ę(zhĻģn)ÓÐŌŧķĻūÖÏÞ�����ĢŽËųÄÜĖáđĐĩÄÐÅÏĒÝ^ÉŲ�ĢŽČËÔÚÕJ(rĻĻn)ŨRĘÂÎïrÍųÍųÐčŌŠēÉÓÃķā·N·Öî·―·Ļ(Čį―ŧēæ·Öî·Ļ)ĢŽíŅa(bĻģ)ÎŌŧ·Öî·―·ĻĩÄēŧŨã��ĢŽĀýČį����ĢŽĶÓÚNa2CO3����ĢŽÄÆä―MģÉĩÄęëxŨÓíŋīĢŽŲÓÚâcû};ķøÄÆä―MģÉĩÄęëxŨÓíŋī���ĢŽtŲÓÚĖžËáû}���ĄĢ
ĄĄĄĄÓÐrĢŽÎïŲ|(zhĻŽ)ŧō·īŠ(yĻĐng)ßM(jĻŽn)ÐÐŌŧīηÖîËųŪa(chĻĢn)ÉúĩÄ―Y(jiĻĶ)đû���ĢŽÏāËÆÐÔßēŧōÃũï@����ĢŽß@rÎŌŋÉŌÔĶÆäÖÐĩÄÃŋŌŧîÎïŲ|(zhĻŽ)ŧō·īŠ(yĻĐng)ßM(jĻŽn)ÐÐÔŲ·ÖîĢŽÐÎģÉļüŋÆW(xuĻĶ)ĩÄÕJ(rĻĻn)ŨR�ĄĢŧŊW(xuĻĶ)ÉÏ���ĢŽÍĻģ���ĢŋÉļųþ(jĻī)ÎïŲ|(zhĻŽ)ĩÄ―MģÉĄĒ îB(tĻĪi)�����ĄĒÐÔŲ|(zhĻŽ)ĩČĶÎïŲ|(zhĻŽ)ßM(jĻŽn)ÐзÖî�����ĄĢĀýČįĢšļųþ(jĻī)ÎïŲ|(zhĻŽ)ĩÄīæÔÚ îB(tĻĪi)�����ĢŽĒÎïŲ|(zhĻŽ)·ÖéâB(tĻĪi)ÎïŲ|(zhĻŽ)�����ĄĒŌšB(tĻĪi)ÎïŲ|(zhĻŽ)šÍđĖB(tĻĪi)ÎïŲ|(zhĻŽ);ļųþ(jĻī)ÎïŲ|(zhĻŽ)ĩħ(dĻĢo)ëÐÔĢŽĒÎïŲ|(zhĻŽ)·Öé§(dĻĢo)ów����ĄĒ°ë§(dĻĢo)ówšÍ―^ūów;ļųþ(jĻī)ÎïŲ|(zhĻŽ)ÔÚËŪÖÐĩÄČÜ―âÐÔĢŽĒÎïŲ|(zhĻŽ)·ÖéŋÉČÜÐÔÎïŲ|(zhĻŽ)��ĄĒÎĒČÜÐÔÎïŲ|(zhĻŽ)šÍëyČÜÐÔÎïŲ|(zhĻŽ)�ĄĢÄW(xuĻĶ)Á(xĻŠ)ÎïŲ|(zhĻŽ)ŧŊW(xuĻĶ)ÐÔŲ|(zhĻŽ)ĩÄÐčŌŠģö°l(fĻĄ)ĢŽÎŌļüÏēgļųþ(jĻī)ÎïŲ|(zhĻŽ)ĩÄ―MģÉšÍÐÔŲ|(zhĻŽ)ĖØüc(diĻĢn)����ĢŽĶÎïŲ|(zhĻŽ)ßM(jĻŽn)ÐзÖî�����ĄĢļųþ(jĻī)―MģÉÎïŲ|(zhĻŽ)ËųšŽ·ÖŨÓ·Nî�����ĢŽŋÉŌÔĒÎïŲ|(zhĻŽ)·ÖģÉžôÎïšÍŧėšÏÎï;ÔŲļųþ(jĻī)―MģÉÔŠËØĩÄ·Nî����ĢŽÓÖŋÉĒžôÎï·ÖģÉÎŲ|(zhĻŽ)šÍŧŊšÏÎï;ļųþ(jĻī)―MģÉÔŠËØĩÄ·NîēŧÍŽĢŽßŋÉĒÎŲ|(zhĻŽ)·ÖģÉ―ðŲÎŲ|(zhĻŽ)šÍ·Į―ðŲÎŲ|(zhĻŽ);ļųþ(jĻī)ĘĮ·ņšŽÓÐĖžÔŠËØÓÖŋÉĒŧŊšÏÎï·ÖģÉÓÐC(jĻĐ)ŧŊšÏÎïšÍoC(jĻĐ)ŧŊšÏÎï……ĀíÕÉÏ�����ĢŽÎŌŋÉŌÔēŧāĩØĶËųĩ÷Öî―Y(jiĻĶ)đûßM(jĻŽn)ÐÐÔŲ·ÖîĢŽß@·N·ÖîęP(guĻĄn)ÏĩŌŧ°ãŋÉÓÃä îDßM(jĻŽn)ÐÐąíĘū����ĢŽËųŌÔß@·N·Öî·―·ĻÓÖ·Qé“ä î·Öî·Ļ”(ÏÂDéŧŊW(xuĻĶ)ÉÏĶÎïŲ|(zhĻŽ)ĩÄģĢŌä î·Öî)ĄĢ
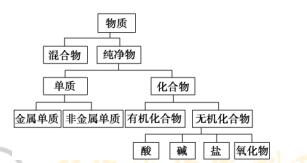
ĄĄĄĄ[ÔŌŧÔ]ĄĄ3.ÓÃä îDąíĘūÏÂÁÐÎïŲ|(zhĻŽ)ĩÄ·ÖîĢšæV(Mg)�ĄĒ ÂČâ(Cl2)ĄĒÂČŧŊčF(FeCl3)ČÜŌš����ĄĒÁōËá(H2SO4)ĄĒÏõËáä^[Ba(NO3)2]����ĄĒČýŅõŧŊķþčF(Fe2O3)ĄĒ äŅõŧŊâc(NaOH)�����ĄĒÆÏĖŅĖĮ(C6H12O6)���ĄĒ ŌŌīž(C2H5OH)���ĄĒĩâūÆ��ĄĒķþŅõŧŊĖž��ĄĢ
ĄĄĄĄŲYÁÏŋĻÆŽĄĄÔÚoC(jĻĐ)Ëá·ÖŨÓÖÐ��ĢŽŌŧ°ã·ÖŨÓÖÐÓÐŨäūÍĘĮŨÔŠËá��ĢŽĩŦÎŌēŧÄÜšÎļųþ(jĻī)ÓÐC(jĻĐ)Ëá·ÖŨÓÖÐHĩ(shĻī)ī_ķĻËüĘĮŨÔŠËá�����ĢŽČįīŨËá(CH3COOH)ÓÐ4H���ĢŽĩŦËüĘĮŌŧÔŠËáĄĢ
ĄĄĄĄÔÚËŪČÜŌšÖÐŪa(chĻĢn)ÉúĩÄęëxŨÓČŦēŋĘĮäëxŨÓĩÄŧŊšÏÎï·QÖŪéËá����ĄĢû}Ëá���ĄĒÁōËá��ĄĒÏõËá���ĄĒĖžËášÍīŨËáĘĮŨ·NŨîģĢŌĩÄËá�ĄĢČËßŋÉŌÔļųþ(jĻī)ËüÔÚ―MģÉ���ĄĒÐÔŲ|(zhĻŽ)ÉÏĩÄēîŪ�����ĢŽßM(jĻŽn)ÐÐļüéž(xĻŽ)ÖÂĩÄ·Ö����ĄĢČįļųþ(jĻī)―MģÉÖÐĘĮ·ņšŽŅõÔŠËØŋÉŌÔ·Ö階ŅõËášÍoŅõËá���ĢŽÁōËá�ĄĒÏõËá�����ĄĒĖžËášÍīŨËáūÍĘĮģĢŌĩÄšŽŅõËá��ĢŽķøû}ËátĘĮoŅõËá;ļųþ(jĻī)ËáŪa(chĻĢn)ÉúäëxŨÓĩÄģĖķČŋÉŌÔ·Öé(qiĻĒng)ËášÍČõËá�����ĢŽČįû}ËáĄĒÁōËá����ĄĒÏõËáĘĮ(qiĻĒng)ËáĢŽķøĖžËá����ĄĒīŨËáĘĮČõËá;ļųþ(jĻī)ÃŋËá·ÖŨÓëëxŪa(chĻĢn)ÉúĩÄäëxŨÓĩ(shĻī)ŋÉŌÔ·ÖéŌŧÔŠËáĄĒķþÔŠËá����ĄĒČýÔŠËáĢŽČįû}Ëá�ĄĒÏõËáĘĮŌŧÔŠËáĢŽÁōËá�����ĄĒĖžËáĘĮķþÔŠËá��ĢŽÁŨËá(H3PO4)ĘĮČýÔŠËá;ļųþ(jĻī)ËáĘĮ·ņūßÓÐ]°l(fĻĄ)ÐÔ�����ĢŽŋÉŌÔ·ÖģÉëy]°l(fĻĄ)ÐÔËášÍ]°l(fĻĄ)ÐÔËá��ĢŽÁōËášÍÁŨËáĘĮëy]°l(fĻĄ)ÐÔËá���ĢŽû}Ëá�ĄĒÏõËá�����ĄĒīŨËáķžĘĮ]°l(fĻĄ)ÐÔËá;ßŋÉŌÔļųþ(jĻī)ÔÚÓÐC(jĻĐ)ŧŊšÏÎïšÍoC(jĻĐ)ŧŊšÏÎïÖÐĩÄwŲ���ĢŽĒËá·ÖéoC(jĻĐ)ËášÍÓÐC(jĻĐ)Ëá�����ĢŽīŨËáĘĮŨîģĢŌĩÄÓÐC(jĻĐ)Ëá����ĢŽÆäËûŌŧ°ãķžĘĮoC(jĻĐ)Ëá��ĄĢ
ĄĄĄĄŲYÁÏŋĻÆŽĄĄĀ(yĻĒn)ļņŌâÁxÉÏÕf���ĢŽû}Ëá���ĄĒ°ąËŪĘĮŧėšÏÎïĢŽēŧÄÜ·QÖŪéËáĄĒA����ĢŽķøŠ(yĻĐng)Ô·QHClĄĒNH3·H2OéËá�����ĄĒA��ĢŽÖŧĘĮČËŌŧÖąŅØÓÃÁ(xĻŠ)TÁË����ĢŽW(xuĻĶ)Á(xĻŠ)ÖÐŌŠŨĒŌâß@ŌŧÁ(xĻŠ)TĄĢ
ĄĄĄĄÔÚËŪČÜŌšÖÐŪa(chĻĢn)ÉúĩÄęëxŨÓČŦēŋĘĮäŅõļųëxŨÓĩÄŧŊšÏÎï·QÖŪéA��ĢŽäŅõŧŊâc�ĄĒäŅõŧŊâ}ĄĒäŅõŧŊã~ĘĮŨ·NÖØŌŠĩÄA����ĄĢĶAßM(jĻŽn)ÐÐÔŲ·ÖîĢŽĒļüžÓÓÐĀûÓÚÎŌĀí―âAĩÄŧŊW(xuĻĶ)ÐÔŲ|(zhĻŽ)��ĄĢŌŧ°ãŋÉļųþ(jĻī)AŪa(chĻĢn)ÉúäŅõļųëxŨÓĩÄëyŌŨģĖķČ·Öé(qiĻĒng)AšÍČõA��ĢŽäŅõŧŊâc���ĄĒäŅõŧŊâ�����ĄĒäŅõŧŊâ}���ĄĒäŅõŧŊä^[Ba(OH)2]ĘĮģĢŌĩÄ(qiĻĒng)AĢŽķøäŅõŧŊčF�����ĄĒäŅõŧŊã~���ĄĒNH3·H2OĘĮģĢŌĩÄČõA;ļųþ(jĻī)ČÜ―âÐÔēîŪŋÉ·ÖéŋÉČÜÐÔA�ĄĒÎĒČÜÐÔAšÍëyČÜÐÔA�ĢŽäŅõŧŊâcĄĒäŅõŧŊâ�ĄĒäŅõŧŊä^ĄĒNH3·H2OĘĮŋÉČÜÐÔA��ĢŽäŅõŧŊâ}ĘĮÎĒČÜÐÔA��ĢŽäŅõŧŊčFĄĒäŅõŧŊã~ĘĮëyČÜÐÔA��Ą�ĢŋÉČÜÐÔŧōÎĒČÜÐÔAŌŧ°ãĘĮ(qiĻĒng)AĢŽŋÉŌÔÓÉĶŠ(yĻĐng)ĩÄ―ðŲŅõŧŊÎïšÍËŪŧŊšÏķøģÉ�ĢŽÔÚžÓálžþÏÂēŧŌŨ·Ö―â;ķøëyČÜÐÔAŌŧ°ãĘĮČõAĢŽÔÚžÓálžþÏÂŋÉŌÔ·Ö―âģÉĶŠ(yĻĐng)―ðŲŅõŧŊÎïšÍËŪ��ĢŽĩŦēŧÄÜÓÉĶŠ(yĻĐng)―ðŲŅõŧŊÎïšÍËŪŧŊšÏķøģÉ����ĄĢ
ĄĄĄĄ[ÏëŌŧÏë]ĄĄÄÜ·ņÍĻß^Ōŧē―·īŠ(yĻĐng)ÍęģÉÏÂÁÐÞD(zhuĻĢn)ŨĢšFe2O3→Fe(OH)3šÍK2O→KOHĄĢ
ĄĄĄĄÓÉ―ðŲęëxŨÓ(ŧōä@ļų)ÅcËáļųëxŨÓ(gĻ°u)ģÉĩÄŧŊšÏÎï·QÖŪéû}����ĄĢĖžËáâ}ĄĒÂČŧŊâc���ĄĒÁōËáã~ķžĘĮÖØŌŠĩÄû}�ĄĢĶû}ĩÄßM(jĻŽn)Ōŧē―·Öî��ĢŽÓÐĀûÓÚÎŌļüšÃĩÄW(xuĻĶ)Á(xĻŠ)û}ĩÄŧŊW(xuĻĶ)ÐÔŲ|(zhĻŽ)�����ĄĢû}ŋÉŌÔŌĀþ(jĻī)―MģÉ·Öéâcû}ĄĒâû}��ĄĒâ}û}ĩČ��ĢŽŌēŋÉŌÔ·Öéû}Ëáû}��ĄĒÁōËáû}���ĄĒÏõËáû}ĄĒĖžËáû}ĩČ;ļųþ(jĻī)ÔÚËŪÖÐĩÄČÜ―âÐÔ·ÖéŋÉČÜÐÔû}�ĄĒÎĒČÜÐÔû}šÍëyČÜÐÔû}ĄĢŌĀþ(jĻī)ËųšŽĩÄ―ðŲęëxŨÓĩÄÃÜķČīóÐĄ���ĢŽÓÖŋÉŌÔ·ÖéÝp―ðŲû}šÍÖØ―ðŲû}��ĢŽBaCl2�ĄĒCuSO4���ĄĒFeCl3ŲÓÚÖØ―ðŲû};ßŋÉŌÔļųþ(jĻī)û}ÄÜ·ņŪa(chĻĢn)ÉúH+ŧōOH-�����ĢŽ°Ņû}·ÖéËáĘ―û}šÍAĘ―û}�ĢŽNaHCO3ĄĒNaHSO4ĘĮģĢŌĩÄËáĘ―û}�����ĢŽCu2(OH)2CO3ĘĮģĢŌĩÄAĘ―û}��ĢŽĶÓÚNaCl�����ĄĒCuSO4ĩČžČ]ÓÐH+Ōē]ÓÐOH-���ĢŽËüąŧ·QéÕýû}�ĢŽģõÖÐŧŊW(xuĻĶ)W(xuĻĶ)Á(xĻŠ)ĩÄû}īóēŋ·ÖķžĘĮß@·NÕýû}�����ĄĢ
ĄĄĄĄ[ÔŌŧÔ]ĄĄ4.Mg(OH)ClŲÓÚû}ßĘĮA?ČįđûĘĮû}ËüÓÖÄÜwŲÓÚÄÄÐĐîÐÍ���ĄĢ
ĄĄĄĄŲYÁÏŋĻÆŽĄĄËŪówÖØ―ðŲëxŨÓÎÛČū���ĢŽĘĮÖļšŽÓÐÖØ―ðŲëxŨÓĩÄÎÛČūÎïßM(jĻŽn)ČëËŪówĶËŪówÔėģÉĩÄÎÛČūĄĢŌąĩV��ĄĒC(jĻĐ)ÐĩÖÆÔėĄĒŧŊđĪ�����ĄĒëŨÓ���ĄĒxąíĩČđĪI(yĻĻ)ÉúŪa(chĻĢn)ß^ģĖÖÐŪa(chĻĢn)ÉúĩÄÖØ―ðŲUËŪ(šŽÓÐãtĄĒæk���ĄĒã~��ĄĒđŊ���ĄĒæĩČÖØ―ðŲëxŨÓ)ĢŽĘĮĶËŪówÎÛČūŨîĀ(yĻĒn)ÖØšÍĶČËîÎĢšĶŨîīóĩÄđĪI(yĻĻ)UËŪÖŪŌŧ���ĄĢUËŪÖÐĩÄÖØ―ðŲëxŨÓĘĮļũ·NģĢÓÃËŪĖĀí·―·ĻēŧÄÜ·Ö―âÆÆÄĩÄ��ĢŽķøÖŧÄÜÞD(zhuĻĢn)ŌÆËüĩÄīæÔÚÎŧÖÚÍÞD(zhuĻĢn)ŨËüĩÄÎïĀíŧŊW(xuĻĶ) îB(tĻĪi)�ĄĢŌōīË�����ĢŽÖØ―ðŲUËŪŠ(yĻĐng)Ū(dĻĄng)ÔÚŪa(chĻĢn)ÉúĩØüc(diĻĢn)ūÍĩØĖĀíĢŽēŧÅcÆäËûUËŪŧėšÏ�ĄĢČįđûÓÚŽÓÐÖØ―ðŲëxŨÓĩÄÎÛÄāšÍUËŪŨũé·ĘÁÏšÍđāļČÞr(nĻŪng)ĖïĢŽþĘđÍÁČĀĘÜĩ―ÎÛČū�ĢŽÔėģÉÞr(nĻŪng)ŨũÎïž°ËŪÉúÉúÎïÖØ―ðŲëxŨÓĩÄļŧžŊĢŽÍĻß^ĘģÎïæŨî―KĶČËówŪa(chĻĢn)ÉúĀ(yĻĒn)ÖØÎĢšĶ��ĄĢ
ĄĄĄĄækÎÛČūĢšŨÔ1995ÄęÆð����ĢŽūÓŨĄÔÚČÕąūļŧÉ―ĘÐÉņÍĻīĻÏÂÓÎĩØ
^(qĻą)ĩÄŌŧÐĐÞr(nĻŪng)ÃņĩÃÁËŌŧ·NÆæđÖĩÄēĄĄĢĩÃēĄģõÆÚ���ĢŽŧžÕßÖŧļÐĩ―Ņü�ĄĒąģšÍĘÖŨãĩČķāĖęP(guĻĄn)đ(jiĻĶ)ĖÛÍī�ĢŽšóí°l(fĻĄ)ÕđéÉņ―(jĻĐng)ÍīĄ�ĢŧžÕßŨßÆð·íÏņøŨÓŌŧÓuu[[ĢŽÍíÉÏËŊÔÚīēÉÏ―(jĻĐng)ģĢÍīĩÃÖąš°“Íī……”ŌōīËß@·NēĄąŧ·Qé“ÍīÍīēĄ”���ĢŽÓÖ·Qé“đĮÍīēĄ”��ĄĢĩÃÁËß@·NēĄ�����ĢŽČËĩÄÉíļßŋsķĖ�ĢŽđĮũĀŨÐÎĄĒŌŨÕÛ�����ĢŽÝpÎĒŧîÓ����ĢŽÉõÖÁŋČËÔŌŧÂĢŽķžŋÉÄܧ(dĻĢo)ÖÂđĮÕÛ�ĢŽŌŧÐĐČËÍīēŧÓûÉú�ĢŽŨÔĒÉíÍöĄĢ―(jĻĐng)ß^Õ{(diĻĪo)ēé����ĢŽÔėģÉß@·N”đĮÍīēĄ“ĩÄÔŌōĘĮÉņÍĻīĻÉÏÓÎĩÄä\SéLÄęĀÛÔÂÅÅ·ÅšŽækĩÄUËŪĢŽŪ(dĻĄng)?shĻī)ØÞr(nĻŪng)ÃņéLÆÚïÓÃĘÜĩ―ækÎÛČūĩÄšÓËŪ���ĢŽēĒĮŌĘģÓÃīËšÓËŪđāļČÉúéLĩÄĩūÃŨ�ĢŽÓÚĘĮækąãÍĻß^ĘģÎïæßM(jĻŽn)ČëČËów�����ĢŽÔÚówČ(nĻĻi)Öðu·eūÛĢŽŌýÆðækÖÐķū�����ĢŽÔėģÉ“đĮÍīēĄ”�ĄĢ
ĄĄĄĄđŊÎÛČūĢšÎåĘŪÄęīúģõÆÚĢŽÔÚČÕąūūÅÖÝÐÜąūŋhËŪRæ(zhĻĻn)�����ĢŽÓÉÓÚČËĘģÓÃĘÜžŨŧųđŊķūšĶĩÄô~îķø§(dĻĢo)ÖžŨŧųđŊÖÐķū�ĢŽ283ČËÖÐķūĢŽÆäÖÐ60ČËËĀÍö���ĄĢ°Y îĢšŋÚýXēŧĮå�����ĄĒē―ÂÄēŧ·(wĻ§n)�ĄĒÃæēŋ°VīôßM(jĻŽn)ķøķúÃ@ŅÛÏđ���ĄĒČŦÉíÂéÄū�ĢŽŨîšóūŦÉņʧģĢĢŽÉíówĮúÖÁËĀÍö�����ĄĢŪa(chĻĢn)ÉúÔŌōĘĮÓÉÓÚđĪSÉúŪa(chĻĢn)ÂČŌŌÏĐšÍīŨËáŌŌÏĐrēÉÓÃÂČŧŊđŊšÍÁōËáŨũīßŧŊĐ���ĢŽŨîšó°ŅšŽÓÐC(jĻĐ)đŊĩÄUËŪ�ĄĒUÔüÅÅČëËŪRģ�����ĢŽĘđô~�ĄĒØĪîĘÜĩ―ÎÛČūĢŽß@ÆðĘžþąŧĘ·W(xuĻĶ)žŌ·Qé“ËŪRĘžþ”���ĄĢ
ĄĄĄĄåiÎÛČūĢšËÄĘŪķāÄęĮ°��ĢŽČÕąūÓÐīåĮf°l(fĻĄ)ÉúÁËŌŧÆðŋÉÅÂĩÄžŊów“°l(fĻĄ)Ŋ”ĘžþĢŽÓÐ16īåÃņÍŧČŧŌŧÆð“°l(fĻĄ)Ŋ”ÁË����ĄĢß@ÐĐ“ŊŨÓ”ŌŧþšŋÞŋÞĖäĖäĢŽŌŧþšÓÖđþđþīóÐĶ;°l(fĻĄ)ŨũrÉĘÖyu��ĢŽîķķēŧÖđĢŽĮŌÏÂÖŦ°l(fĻĄ)Óē―ĐÖą�ĢŽČįīË·īÍ(fĻī)°l(fĻĄ)ŨũĢŽÖąÖÁ“ŊËĀ”����ĄĢÕ{(diĻĪo)ēé°l(fĻĄ)ŽF(xiĻĪn)ß@ÐĐČËšČĩÄĘĮÍŽŌŧŋÚËŪūŪÖÐĩÄËŪĢŽŋžēėËŪūŪ���ĢŽÓÖÔÚÅÔß
ÍÚģöÁËīóÁŋUÅf����ĄĒÆÆ ĩÄļÉëģØ���ĄĢÔíß@ĘĮËŪūŪĘÜļÉëģØÖÐÄģÐĐÓКĶģÉ·ÖÎÛČūķøÔėģÉĩÄ��ĄĢþ(jĻī)h(huĻĒn)ūģŋÆW(xuĻĶ)žŌŅÐūŋąíÃũ����ĢŽUÅfļÉëģØÖÐĩÄä\����ĄĒķþŅõŧŊåiĩČģÉ·ÖéLÆÚÂņÔÚĩØÏÂĢŽþÅcÍÁČĀÖÐŧŊW(xuĻĶ)ÎïŲ|(zhĻŽ)°l(fĻĄ)ÉúŨũÓÃ��ĢŽÉúģÉä\åiËáĘ―û}ĢŽËüBČëĩØÏÂ���ĢŽOŌŨÎÛČūïÓÃËŪ���ĢŽķøß@ŌŧČšīåÃņÕýĘĮéLÆÚïÓÃß@·NËŪĢŽÔėģÉÐî·eÐÔåiÖÐķū�����ĢŽēÅÓÐÉÏĘö“°l(fĻĄ)Ŋ”°Y î��ĄĢ
ĄĄĄĄļÉëģØÔÚÖÆÔėß^ģĖÖÐßĘđÓÃŌŧķĻÁŋĩÄđŊ�ĢŽšŽđŊŨîķāĩÄĘĮä\đŊëģØĢŽļßß_(dĻĒ)20% ĄŦ30%�ĢŽAÐÔļÉëģØžsé13%ĢŽÆÕÍĻä\åiëģØšŽđŊÝ^ÉŲ���ĄĢŌōīËļÉëģØēŧHĘĮåiÎÛČūÔī�����ĢŽÍŽrßĘĮđŊÎÛČūÔīĢŽÔÚÏíĘÜļÉëģØ―oÎŌÉúŧî§íąãĀûĩÄÍŽr�����ĢŽąØíęP(guĻĄn)ŨĒUÅfëģØĶh(huĻĒn)ūģĩÄÎĢšĶĢŽēÉČĄĮÐ(shĻŠ)ÓÐЧĩÄŧØĘÕ·―·Ļ��ĢŽŌÔpÝpëģØĶh(huĻĒn)ūģĩÄÎĢšĶ���ĄĢþ(jĻī)―y(tĻŊng)Ó(jĻŽ)���ĢŽÎŌøÃŋÄęÉúŪa(chĻĢn)ļÉëģØ50|ÖŧĢŽÆäÖÐä\đŊëģØšÍAÐÔëģØ1|Öŧ����ĢŽÃŋÄęëģØÓÃđŊ100ĢŽČËÁ(xĻŠ)TÓÃÍęëģØšóëSŌâyG���ĢŽČÕņÓęÁÜŧōÂņČëĩØÏÂÍųÍųÎÛČūh(huĻĒn)ūģ��ĢŽUÅfëģØŧØĘÕĘĮÄŋĮ°ÎŌąØí―âQĩÄŌŧÖØŌŠh(huĻĒn)ūģî}�����ĄĢ
ĄĄĄĄķþŅõŧŊĖž���ĄĒŌŧŅõŧŊĖž�ĄĒËŪ�ĄĒŅõŧŊã~ĄĒŅõŧŊâ}�ĄĒŅõŧŊæVĄĒËÄŅõŧŊČýčFĩČķžĘĮģĢŌĩÄŅõŧŊÎï��ĢŽēŧÍŽŅõŧŊÎïÐÔŲ|(zhĻŽ)žČÓÐÏāÍŽüc(diĻĢn)�ĢŽŌēÓÐēŧÍŽüc(diĻĢn)ĢŽĶŅõŧŊÎïßM(jĻŽn)Ōŧē―·Öî��ĢŽÓÐÖúÓÚÕŌģöļũîÎïŲ|(zhĻŽ)ĩÄŧųąūÍĻÐÔ����ĄĢŌŧ°ãŅõŧŊÎïŋÉŌÔ°ī―MģÉ·Öé―ðŲŅõŧŊÎïšÍ·Į―ðŲŅõŧŊÎïĢŽČįCO��ĄĒCO2�����ĄĒSiO2ūÍĘĮ·Į―ðŲŅõŧŊÎï����ĢŽMn2O7ĄĒCuOĄĒFe2O3ūÍĘĮ―ðŲŅõŧŊÎï����ĄĢÁíŌŧ·NģĢÓ÷―·ĻĘĮļųþ(jĻī)ŅõŧŊÎïÄÜ·ņšÍËá�ĄĒA·īŠ(yĻĐng)ÉúģÉû}šÍËŪĢŽĒÆä·ÖģÉēŧģÉû}ŅõŧŊÎïšÍģÉû}ŅõŧŊÎï�ĢŽČįCOĄĒNOéēŧģÉû}ŅõŧŊÎï��ĢŽķøCO2����ĄĒSiO2ĄĒCuO��ĄĒFe2O3éģÉû}ŅõŧŊÎï���ĄĢļųþ(jĻī)ģÉû}ŅõŧŊÎïšÍËá�ĄĒA·īŠ(yĻĐng)ĩÄŋÉÄÜÐÔÓÖŋÉ·ÖģÉēŧÍŽîÐÍ����ĢŽÅcA·īŠ(yĻĐng)ÉúģÉû}šÍËŪĩÄŅõŧŊÎï·QéËáÐÔŅõŧŊÎïĢŽČįCO2���ĄĒSiO2;ÅcËá·īŠ(yĻĐng)ÉúģÉû}šÍËŪĩÄŅõŧŊÎï·QéAÐÔŅõŧŊÎï�ĢŽČįCaOĄĒNa2O��ĄĢ
ĄĄĄĄCO2+Ca(OH)2===CaCO3↓+H2O
ĄĄĄĄMn2O7+2KOH===2KMnO4+H2O
ĄĄĄĄCaO+2HCl===CaCl2+H2O
ĄĄĄĄCuO+H2SO4===CuSO4+H2O
ĄĄĄĄ[ÔŌŧÔ]ĄĄ5.ēŧÍŽ·Öî―Y(jiĻĶ)đûÖŪégĩÄwŲęP(guĻĄn)Ïĩ�����ĢŽĘĮŅõŧŊÎïļÅÄîĩÄŋžēéÖØüc(diĻĢn)�ĢŽÄĮÃī―ðŲŅõŧŊÎïŌŧķĻĘĮAÐÔŅõŧŊÎïá?ËáÐÔŅõŧŊÎïŌŧķĻĘĮ·Į―ðŲŅõŧŊÎïá?
ĄĄĄĄĘÂ(shĻŠ)ÉÏĢŽÓÐÐĐŅõŧŊÎïēŧĩŦŋÉŌÔšÍËá·īŠ(yĻĐng)ÉúģÉû}šÍËŪ���ĢŽŌēŋÉŌÔšÍA·īŠ(yĻĐng)ÉúģÉû}šÍËŪ�����ĢŽß@·NŅõŧŊÎïūÍąŧ·QéÉÐÔŅõŧŊÎï�����ĢŽŅõŧŊäXĘĮÆäÖÐĩÄĩäÐÍīúąí����ĄĢ
ĄĄĄĄAl2O3+6HCl===2AlCl3+3H2O
ĄĄĄĄAl2O3+2NaOH===2NaAlO2+H2O(NaAlO2·QéÆŦäXËáâc)
ÐÂģõČýŋėßīaęP(guĻĄn)ŨĒ
ÖÐŋžūW(wĻĢng)ÎĒÐÅđŦąĖ
ÃŋČÕÍÆËÍW(xuĻĶ)Á(xĻŠ)žžĮÉ�����ĢŽW(xuĻĶ)ŋÆÖŠŨRüc(diĻĢn)
ÖúÄãÓ―Ó2020ÄęÖÐŋžĢĄ
ĄĄĄĄ gÓĘđÓÃĘÖC(jĻĐ)��ĄĒÆ―°åĩČŌÆÓÔO(shĻĻ)äÔLÖÐŋžūW(wĻĢng)���ĢŽ2024ÖÐŋžŌŧ·Åã°éÍŽÐÐĢĄ>>üc(diĻĢn)ôēéŋī












