一����、酸及酸的通性
酸的定義����,電離時(shí)生成的陽(yáng)離子全部都是H+。酸是由氫離子和酸根離子構(gòu)成����。
1.濃鹽酸、濃硫酸的物理性質(zhì)���、特性�、用途
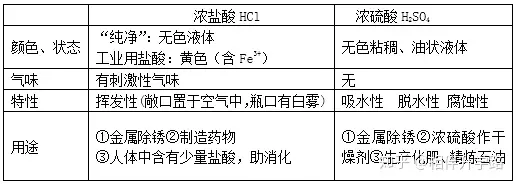
2.酸的通性:鹽 酸 HCl 硫 酸 H2SO4
酸使紫色石蕊試液變紅�����,使無(wú)色酚酞試液不變色�。
金屬+酸→鹽+氫氣
Zn+2HCl=ZnCl2+H2↑
Zn+ H2SO4 =ZnSO4+H2↑
堿性氧化物+酸→鹽+水
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
堿+酸→鹽+水
NaOH+HCl=NaCl+ H2O
Cu(OH)2+H2SO4= CuSO4+2H2O
鹽+酸→另一種鹽+另一種酸
AgNO3+HCl=AgCl↓+HNO3
BaCl2+H2SO4=BaSO4↓ +2HCl
注意:(1)在‘金屬+酸→鹽+氫氣’中�����,酸通常指的是稀硫酸和稀鹽酸����,不能是濃硫酸或硝酸��。
因?yàn)闈饬蛩峄蛳跛岫加袕?qiáng)氧化性��,與金屬反應(yīng)時(shí)不能生成氫氣而生成了水�。
(2)通過(guò)金屬跟酸的反應(yīng)情況導(dǎo)出金屬活動(dòng)順序表:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金屬活動(dòng)性由強(qiáng)逐漸減弱金屬活動(dòng)性順序中�����,金屬位置越靠前�����,活動(dòng)性越強(qiáng)��,反應(yīng)越劇烈��,所需時(shí)間越短��。
(3)濃硫酸具有吸水性,通常用它作為干燥劑��。
硫酸還具有脫水性���,它對(duì)皮膚或衣服有很強(qiáng)的腐蝕性�����。
稀釋濃硫酸時(shí)一定要把濃硫酸沿著器壁慢慢地注入水里���,并不斷攪動(dòng),切不可把水倒進(jìn)濃硫酸里�,如果把水注入濃硫酸里,水的密度較小��,會(huì)浮在硫酸上面�����,溶解時(shí)放出的熱會(huì)使水立刻沸騰��,使硫酸液向四處飛濺��,容易發(fā)生事故�。
二�、堿及堿的通性
定義:電離時(shí)生成的陰離子全部是OH-離子�����。堿是由金屬離子(或銨根離子)和氫氧根離子構(gòu)成���。
1.氫氧化鈉��、氫氧化鈣的物理性質(zhì)����、用途
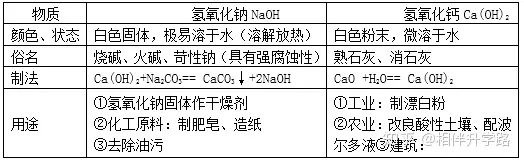
2.堿的通性
堿使紫色石蕊試液變藍(lán)����,使無(wú)色酚酞試液變紅。
氫氧化鈉使紫色石蕊試液變藍(lán)��,無(wú)色酚酞試液變紅��。
氫氧化鈣使紫色石蕊試液變藍(lán)���,無(wú)色酚酞試液變紅。
酸性氧化物+堿→鹽+水
2NaOH+CO2=Na2CO3+H2O Ca(OH)2+CO2=CaCO3↓+H2O
酸+堿→鹽+水
NaOH+HCl=NaCl+H2O
Ca(OH)2+H2SO4= CaSO4+2H2O
鹽+堿→另一種鹽+另一種堿
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
注意:(1)只有可溶性堿才能跟一些非金屬氧化物發(fā)生反應(yīng)��,這些非金屬氧化物是酸性氧化物。酸性氧化物多數(shù)能溶于水�����,跟水化合生成酸�����。
(2)鹽和堿反應(yīng)時(shí)��,必須兩者都是可溶的�,且生成物之一是沉淀,反應(yīng)才能進(jìn)行���。
(3)書(shū)寫(xiě)堿跟某些金屬氧化物反應(yīng)的化學(xué)方程式
關(guān)于這類(lèi)反應(yīng)化學(xué)方程式的書(shū)寫(xiě)有同學(xué)感到很困難�����,為此����,可先寫(xiě)出非金屬氧化物跟水反應(yīng)�����,生成含氧酸的化學(xué)方程式,再以含氧酸和堿相互交換成分寫(xiě)出生成物�����。兩式合并成一個(gè)化學(xué)方程式���。
三���、常見(jiàn)的鹽及鹽的性質(zhì)
1.常見(jiàn)的鹽
定義:能解離出金屬離子(或NH4+)和酸根離子的化合物。
注:此時(shí)的鹽不是指食鹽���,食鹽的主要成分是NaCl����。
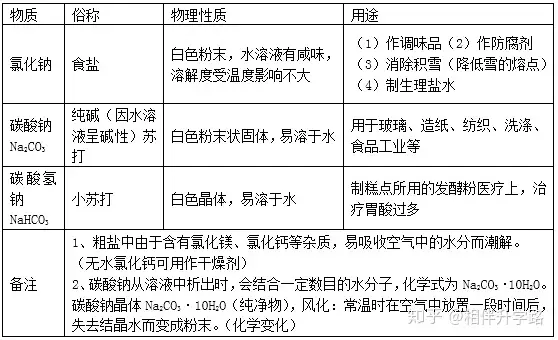
2.精鹽提純
去除不溶性雜質(zhì)���,得到的精鹽中還含有氯化鎂����、氯化鈣等可溶性雜質(zhì)�����。
(1)實(shí)驗(yàn)步驟:溶解����、過(guò)濾、蒸發(fā)

(2)實(shí)驗(yàn)儀器
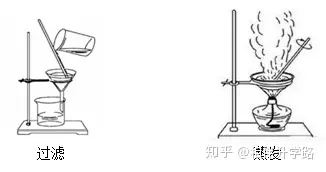
注意:
① 蒸發(fā)皿是可以直接加熱的儀器����,液體體積不能超過(guò)蒸發(fā)皿2/3.
② 溶解時(shí)用玻璃棒攪拌,目的是加快溶解��。
③ 加熱時(shí)用玻璃棒攪拌�,防止局部溫度過(guò)高造成液滴飛濺
④ 待蒸發(fā)皿中出現(xiàn)較多固體時(shí)停止加熱,利用余熱使濾液蒸干�,不能將濾液完全蒸干才停對(duì)于止加熱。
3.鹽的化學(xué)性質(zhì)
鹽溶液+金屬→鹽ˊ+金屬ˊ
CuSO4+Zn= ZnSO4+Cu
鹽+酸→鹽ˊ+ 酸ˊ
BaCl2+H2SO4=BaSO4↓ +2HCl
鹽溶液+堿溶液→鹽ˊ+堿ˊ
3NaOH+FeCl3=3NaCl+Fe(OH)3 ↓
鹽溶液+鹽溶液→鹽ˊ+鹽ˊ
AgNO3+NaCl=AgCl↓+NaNO3
注意:在金屬活動(dòng)順序表中����,只有排在前面的金屬才能把排在后面的金屬?gòu)乃鼈兊柠}溶液中置換出來(lái)。但K���、Ca�����、Na三種金屬與鹽溶液的反應(yīng)特殊�,這里不要求。
四�、復(fù)分解反應(yīng)和酸堿鹽反應(yīng)
1.復(fù)分解反應(yīng)
復(fù)分解反應(yīng)的定義是:由兩種化合物相互交換成分,生成另外兩種化合物的反應(yīng)��。
通式:AB+CD=AD+CB
2.發(fā)生的條件
兩種物質(zhì)在溶液中相互交換離子�,生成物中如果有沉淀析出、氣體放出或有水生成�����,復(fù)分解反應(yīng)均可以發(fā)生����。
3.堿與酸性氧化物反應(yīng)不屬于復(fù)分解反應(yīng)
五、熟記酸�����、堿�、鹽的溶解性
酸、堿�����、鹽的溶解性記憶口訣:
堿中氨�、鉀、鈉��、鋇�、鈣可溶
鉀鈉銨鹽硝酸鹽, 全部都屬可溶鹽�。
硫酸鹽不溶鋇和鉛;
氯化物不溶銀亞汞, 碳酸鹽除鉀鈉銨溶���,其它不溶��。
六�����、幾個(gè)常見(jiàn)離子的檢驗(yàn)
1.Cl-離子的檢驗(yàn)
(分別為實(shí)驗(yàn)操作 實(shí)驗(yàn)現(xiàn)象 實(shí)驗(yàn)結(jié)論 化學(xué)方程式)
取少量樣品于試管中���,滴加AgNO3溶液和稀HNO3
有不溶于稀硝酸的白色沉淀生成
樣品含有Cl-
AgNO3+KCl=AgCl↓+KNO3
2.SO42-離子的檢驗(yàn)
取少量樣品于試管中,滴加Ba(NO3)2溶液和稀HNO3
有不溶于稀硝酸的白色沉淀生成
樣品含有SO42-
Ba(NO3)2+H2SO4=BaSO4↓+2HNO3
3. CO32-離子的檢驗(yàn)
取少量樣品于試管中���,滴加稀HCl,將生成的氣體通入澄清石灰水
有無(wú)色氣體生成�����,該氣體使澄清石灰水變渾濁
樣品含有CO32-
K2CO3+2HCl=2KCl+ CO2↑+H2O
CO2+Ca(OH)2= CaCO3↓+ H2O
4.檢驗(yàn)NH4+
取少量待檢物于潔凈的試管中�����,滴入適量NaOH溶液并加熱��,有使?jié)竦募t色石蕊試紙變成藍(lán)色的氣體產(chǎn)生���。
5.鑒別稀鹽酸和稀硫酸
分別取少量待檢液體于兩支潔凈的試管中����,各滴入幾滴BaCl2溶液�����,有白色沉淀產(chǎn)生的原溶液是稀硫酸�����,無(wú)現(xiàn)象產(chǎn)生的原溶液是稀鹽酸����。
七、常見(jiàn)元素和原子團(tuán)的化合價(jià)
(正價(jià))一氫鉀鈉銀�,二鈣鎂鋇鋅����,三鋁����、四硅��、五氮磷����。
(負(fù)價(jià))負(fù)一價(jià):氟、氯�、溴、碘;
負(fù)二價(jià):氧和硫����。
(可變正價(jià)):一二銅汞,二三鐵���,二四碳�����,四六硫����。
原子團(tuán)的化合價(jià):
負(fù)一價(jià):氫氧根(OH),硝酸根(NO3)����,氯酸根(ClO3),高錳酸根(MnO4);
負(fù)二價(jià):硫酸根(SO4)�����,碳酸根(CO3)�,亞硫酸根(SO3),錳酸根(MnO4);
負(fù)三價(jià):磷酸根(PO4); 正一價(jià):銨根(NH4)�����。
八����、熟記俗稱(chēng)、主要成分和化學(xué)式
生石灰—— CaO
熟石灰——Ca(OH)2
石灰石���、大理石—— CaCO3
食鹽——NaCl
火堿��、燒堿�����、苛性鈉—— NaOH
純堿�、蘇打——Na2CO3
小蘇打—— NaHCO3
鐵銹、赤鐵礦——Fe2O3
赤鐵礦—— Fe3O4
金剛石�����、石墨—— C
干冰——CO2
冰—— H2O
天然氣(甲烷)——CH4
酒精(乙醇)—— C2H5OH
醋酸(乙酸)——CH3COOH
九�����、常見(jiàn)物質(zhì)的顏色
紅色的固體——Cu��、Fe2O3 ��、P(紅磷)
黑色的固體——C�、CuO�、Fe3O4、FeO����、MnO2
白色的固體——KClO3、P2O5、P(白磷)�、CuSO4(無(wú)水硫酸銅)、KCl�����、NaCl等
暗紫色的固體——KMnO4
黃色的固體—— S
藍(lán)色的固體——CuSO4•5H2O
藍(lán)色沉淀——Cu(OH)2
紅褐色沉淀——Fe(OH)3
常見(jiàn)不溶于酸的白色沉淀——BaSO4����、AgCl
溶于酸并放出使澄清石灰水變渾濁的氣體的白色沉淀——BaCO3、CaCO3
溶于酸但不產(chǎn)生氣體的白色沉淀——Mg(OH)2���、Al(OH)3等不溶性堿的沉淀
藍(lán)色的溶液—— CuSO4���、CuCl2、Cu(NO3)2等含Cu2+溶液
淺綠色的溶液——FeSO4���、FeCl2等含F(xiàn)e2+溶液
黃色的溶液——FeCl3��、Fe2(SO4)3���、Fe(NO3)3等含F(xiàn)e3+溶液
補(bǔ)充下列反應(yīng)方程式:
1.氫氧化銅跟稀鹽酸反應(yīng): Cu(OH)2 + 2HCl = CuCl2 + 2H2O 藍(lán)色沉淀消失
2.氫氧化銅跟稀硫酸反應(yīng): Cu(OH)2 + H2SO4 = CuSO4 + 2H2O 變成藍(lán)色溶液
3.氫氧化鈉跟硫酸銅溶液反應(yīng):2NaOH + CuSO4 = Na2SO4 + Cu(OH)2 ↓ 有藍(lán)色沉淀產(chǎn)生
4.氫氧化鈉跟氯化鐵溶液反應(yīng):3NaOH + FeCl3 = Fe(OH)3↓ +3NaCl 有紅褐色沉淀產(chǎn)生
判斷溶液的酸堿性
用指示劑,溶液的酸堿度——用pH來(lái)表示���。
干燥劑的選擇
1.濃硫酸可干燥:
酸性氣體(如:CO2�����、SO2��、SO3����、NO2、HCl���、)
中性氣體(如:H2��、O2、N2���、CO)
※不能干燥堿性氣體(如:NH3)
2.氫氧化鈉固體���、生石灰、堿石灰可干燥:
堿性氣體(如:NH3)
中性氣體(如:H2���、O2�����、N2��、CO)
※不能干燥酸性氣體(如:CO2����、SO2、SO3����、NO2、HCl)
3.無(wú)水硫酸銅固體遇水由白色變藍(lán)色�,可檢驗(yàn)水的存在,并吸收水蒸氣��。
歡迎使用手機(jī)�����、平板等移動(dòng)設(shè)備訪問(wèn)中考網(wǎng)�,2024中考一路陪伴同行!>>點(diǎn)擊查看














